Definition
Nierenkrebserkrankungen haben in den letzten Jahren in Deutschland deutlich zugenommen. Sowohl die Möglichkeiten der operativen Behandlung als auch die der medikamentösen Therapie haben sich sehr verändert. Während vor einigen Jahren nur eine Totalentfernung der Niere bei einem Tumor möglich war, nehmen heute die Teilentfernung und minimal-invasive Operationsmethoden (laparoskopische Tumornephrektomie und laparoskopische Nierenteilresektion) einen zunehmenden Stellenwert ein. Bei der medikamentösen Behandlung fortgeschrittener Erkrankungen sind durch die Zulassung neuer Substanzen (Avastin®, Sutent®, Nexavar®, Torisel®, Afinitor®, Votrient® und Inlyta®) deutlich individuellere Behandlungsansätze möglich.
Die Nieren liegen gut geschützt im hinteren Bauchraum. Sie sind jedoch so tief gelegen, dass sie sich in der Regel einer Tastuntersuchung entziehen. Durch die weithin zugängliche Ultraschalluntersuchung werden heutzutage die meisten Tumoren an der Niere frühzeitig entdeckt und können so einem heilenden Verfahren zugeführt werden.
Die meisten Tumoren der Niere sind bösartig. Sie können überall in der Niere entstehen. Je nachdem, in welchem Gewebe der Tumor seinen Ursprung nimmt, unterscheidet man verschiedene Formen von Nierenkrebs.
Die häufigsten bösartigen Nierentumoren sind die Nierenzellkarzinome. Sie werden gelegentlich auch Nierenkarzinom oder Adenokarzinom der Niere genannt. Nicht mehr gebräuchlich sind die Begriffe Hypernephrom und Grawitz-Tumor. Sie machen rund 95 % aller Nierentumore aus und gehen von den Zellen der Harnkanälchen (Tubulussystem) aus. Deutlich seltener ist das Onkozytom. Dabei handelt es sich um einen Tumor, der nur örtlich verdrängend wächst, aber keine Absiedlungen (Metastasen) setzt. Das Nierenzellkarzinom wird zusätzlich noch nach dem Wachstumsmuster in klarzellig, chromophob, chromophil, onkozytär und den ducuts Bellini Typ unterschieden.
Sehr viel seltener sind alle anderen bösartigen Tumoren der Niere. Dabei unterscheidet man die vom Gewebe des Nierenbeckens ausgehenden Urothelkarzinome von anderen bösartigen Tumoren, die nicht vom Nierengewebe ausgehen, wie zum Beispiel Lymphome – also Krebserkrankungen des lymphatischen Gewebes – und Sarkome, die sich in Muskulatur, Fett oder Bindegewebe entwickeln. Im Folgenden werden nur noch die Nierenzellkarzinome behandelt, wegen deren wesentlich größerer Häufigkeit.
In der Regel ist nur eine der beiden Nieren von einer Tumorerkrankung betroffen. Nur sehr selten sind gleichzeitig beide Nieren betroffen. Allerdings entwickelt sich im Langzeitverlauf bei etwa 1,5 % der Patienten in beiden Nieren ein Karzinom. In diesen Fällen liegt meist eine genetische Veranlagung für Nierenkrebs vor. Sie ist den Betroffenen häufig schon durch andere Begleiterkrankungen bekannt.
Bau und Funktion der Nieren
Zu den wichtigsten Funktionen der Nieren gehören die Entgiftung des Körpers und die Regulierung des Wasserhaushaltes des Körpers. Bei der Entgiftung werden nicht weiter vom Körper verwendbare Stoffe, sogenannte Endprodukte des Stoffwechsels, aus dem Blut in den Harn ausgeschieden. Die Nieren sind außerdem für die Bildung verschiedener Hormone verantwortlich.
Häufigkeit
Nierenkrebs ist bei den Männern die sechsthäufigste und bei den Frauen die elfthäufigste Tumorerkrankung in der Bundesrepublik Deutschland. Etwa vier bis acht von 100.000 Menschen sind pro Jahr betroffen. Im Jahr 2002 erkrankten in Deutschland nach Schätzungen des Robert-Koch-Instituts 10.300 Männer und 6.400 Frauen neu an Nierenkrebs. In diesen Zahlen enthalten sind allerdings auch die selteneren Urothel-Karzinome des Nierenbeckens und des Harnleiters.
Von allen bösartigen Tumorerkrankungen machen die Nierenkarzinome nahezu vier Prozent aus. Allerdings beobachtet man in den letzten zehn Jahren weltweit eine Zunahme dieser Krebsform. Nierenkrebs wird besonders häufig zwischen dem 40. und 60. Lebensjahr diagnostiziert. Jüngere Menschen sind deutlich seltener betroffen. Das mittlere Erkrankungsalter liegt bei Männern bei etwa 63, bei Frauen bei etwa 67 Jahren. Männer erkranken etwa 1,5-mal häufiger als Frauen.
Durch den umfassenden Einsatz der Ultraschalluntersuchung werden heute die meisten Neuerkrankungen schon in einem frühen Stadium diagnostiziert, sodass zumeist Heilungen erreicht werden können. In fortgeschrittenen Krankheitsstadien sind die Heilungsaussichten jedoch sehr ungünstig.
Ursachen
Die genauen Ursachen für die Entstehung von Nierenkrebs sind weitgehend unbekannt. Einigen Substanzen wird die Entstehung von Nierenkrebs angelastet. So tritt z.B. nach der Einwirkung ionisierender Strahlen und langjähriger Einwirkung von Asbest, Cadmium (z. B. aus NiCd Batterien), oder Produkten aus der Lösungsmittel- und Ölverarbeitenden Industrie Nierenkrebs mit höherer Wahrscheinlichkeit auf. Ebenso gelten Zigarettenrauch und chronischer Funktionsverlust der Nieren als Risikofaktoren. In seltenen Fällen entsteht Nierenkrebs als Folge von genetischen Veränderungen. Hier sind insbesondere die von-Hippel-Lindau’sche Erkrankung und die tuberöse Sklerose zu nennen. Bei den betroffenen Patienten ist mit einer erheblich erhöhten Wahrscheinlichkeit des Auftretens von Nierenzellkarzinomen zu rechnen und hier sind regelmäßige (z.B. jährliche) Früherkennungsuntersuchungen äußerst sinnvoll. Insbesondere ist eine ausführliche Beratung erforderlich. Nierenzellkarzinome können sich frühzeitig über die Lymph- und Blutgefäße im Körper ausbreiten; sie bilden Metastasen in den Lymphknoten und verschiedenen Organen. Besonders häufig betroffen sind die Lunge, Knochen, Leber und das Gehirn. Auch in der zweiten Niere auf der gegenüberliegenden Seite können sich Metastasen absiedeln.
Symptome
Beim Nierenzellkarzinom gibt es keine Frühsymptome. Erste Anzeichen treten meist erst bei sehr fortgeschrittener Erkrankung auf. In diesem Stadium sind folgende Symptome möglich:
Diagnostik
Weit mehr als die Hälfte aller Tumoren der Nieren werden zufällig im Rahmen einer Ultraschalluntersuchung, einer Computer-Tomographie oder Kernspin-Untersuchung entdeckt. Oft ist die Ultraschalluntersuchung schon eindeutig im Nachweis eines Tumors an der Niere. Zur Planung der weiteren Behandlung sind jedoch oft Zusatzuntersuchungen notwendig. Insbesondere, wenn operative Maßnahmen geplant werden und bereits vor der Operation festgelegt werden muss, ob ein nierenerhaltendes Vorgehen möglich ist oder ob die gesamte Niere entfernt werden muss, sind exakte Informationen über Ausdehnung und eventuelle Beteiligung weiterer Organe wichtig.
An weiteren bildgebenden Untersuchungen zur örtlichen Ausdehnung des Tumors sind verfügbar:
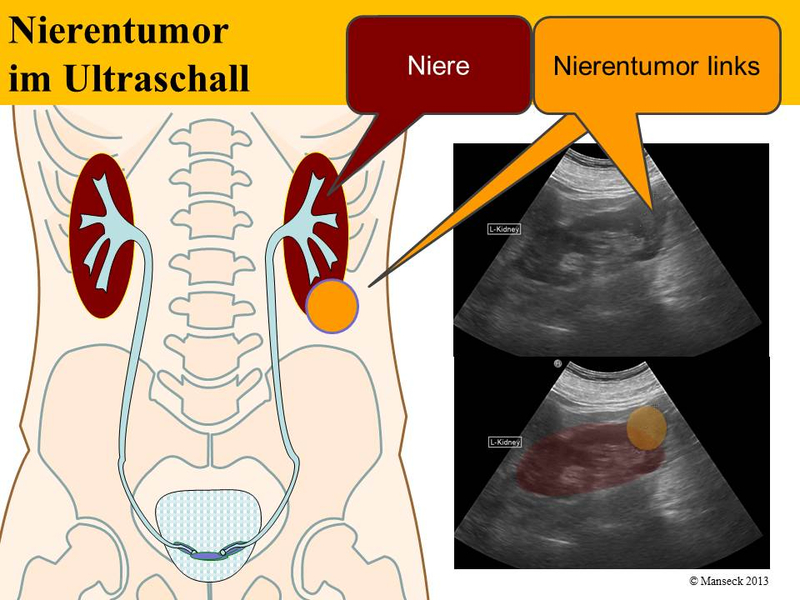
Nierentumor linker Unterpol
Therapie
Die bestmögliche Behandlung bei Nierenkrebserkankung ist die vollständige Entfernung des Tumors. Während dies früher nahezu ausschließlich per Schnitt erfolgte, gewinnen heute die minimal-invasiven und roboter-unterstützten Operationsverfahren zunehmend an Bedeutung. Daneben kommt der Überlegung hinsichtlich radikaler Entfernung der gesamten Niere und organerhaltender Nierenchirurgie breiter Raum zu.
Örtlich begrenzte Nierentumore
Die vollständige Entfernung des Tumors der Niere und ggf. der umgebenden Lymphknoten ist bis heute die einzige Therapie, die zur Heilung führt. Strahlen-, Chemo- und Hormontherapie haben sich in der Vergangenheit als nahezu völlig wirkungslos erwiesen. Vor allem bei Patienten ohne Fernmetastasen bietet einzig die Operation die Chance auf eine Heilung.
An operativen Maßnahmen steht mittlerweile eine ganze Palette an Möglichkeiten in der Urologischen Klinik zur Verfügung. Während vor noch wenigen Jahren nahezu in jedem Fall die gesamte Niere entfernt wurde, haben heute die organerhaltenden Operationen einen sehr großen Stellenwert eingenommen.
Bei kleineren Tumoren bis vier Zentimeter Durchmesser kann beinahe immer der nicht betroffene Anteil der Niere erhalten werden. Bei größeren Tumoren muss in jedem Einzelfall überprüft werden, ob ein Teil der Niere gerettet werden kann, oder die gesamte Niere entfernt werden muss. Nur bei großen und sehr großen Tumoren muss in jedem Fall die gesamte Niere, mit Fettkapsel und Nebenniere sowie den zugehörigen Lymphknoten entfernt werden. Neben den klassischen, offen operativen Zugangswegen über Bauch- oder Flankenschnitt, werden in der Urologischen Klinik zunehmend auch minimal-invasive Operationen (Laparoskopie oder Knopflochchirurgie) sowie roboter-unterstützte Operationen (sogenannte Da Vinci Nephrektomie oder Da Vinci partielle Nephrektomie) eingesetzt. Eine weit überregionale Besonderheit der Urologischen Klinik ist, dass speziell bei der minimal-invasiven Operation an der Niere zwei Zugangswege routinemäßig etabliert sind. So wird sowohl transperitoneal (d.h. durch die Bauchhöhle) als auch retroperitoneal (d.h. ohne Eröffnung der Bauchhöhle, alleine im hinteren Bauchraum) vorgegangen. So kann bei jedem Patienten individuell gehandelt werden. In Abhängigkeit vom Sitz des Tumors und dessen Größe sowie auch unter Berücksichtigung von Voroperationen, die Eingriffe über die Bauchhöhle oft erschweren oder sogar unmöglich machen können, wird für jeden Patienten individuell der bestmögliche operative Zugang gewählt. Spezielle Expertise besteht in der Behandlung von örtlich sehr ausgedehnten Tumoren mit Beteiligung umliegender Organe oder Bildung von Tumorzapfen in Nierenvene oder unterer Hohlvene. Das interdisziplinäre Umfeld gestattet hier eine optimale Betreuung unter Beteiligung aller Organspezialisten.
Bei sehr großen Tumoren, wegen ihrer Ausdehnung und möglichen Blutungskomplikationen, oder einem unvertretbar hohem Operationsrisiko für schwerkranke Patienten, kann ein Verschluss (Embolisation) der Nierenarterie hilfreich sein. Darunter versteht man den Verschluss des zuführenden Blutgefäßes zur Niere. Die Embolisation der Niere erfolgt radiologisch über einen Katheter, der unter Röntgenkontrolle von der Leiste in die Nierenarterie vorgeschoben wird. Diese wird dann durch kleine Metallspiralen verschlossen, sodass die Blutversorgung des Tumors unterbrochen wird. Der Tumor kann nicht weiter wachsen oder bildet sich sogar zurück. Leider ist die Wirkung zumeist nicht dauerhaft, da sich der Tumor neue Wege zur Blutversorgung schafft.
In sehr ausgewählten Fällen, zum Beispiel bei hochbetagten Menschen oder bei Patienten mit unkalkulierbar hohem Operationsrisiko, steht im Klinikum eine weitere Behandlung zur Verfügung. Bei der sogenannten Radiofrequenzablation (RFA) wird eine Spezialnadel in den Tumor eingebracht. Dies erfolgt unter CT Kontrolle. Dann wird durch Radio-Frequenz Ablation das Tumorgewebe durch Überhitzung zerstört. Auch dieses Verfahren stellt ähnlich wie die Embolisation keine Heilung dar.
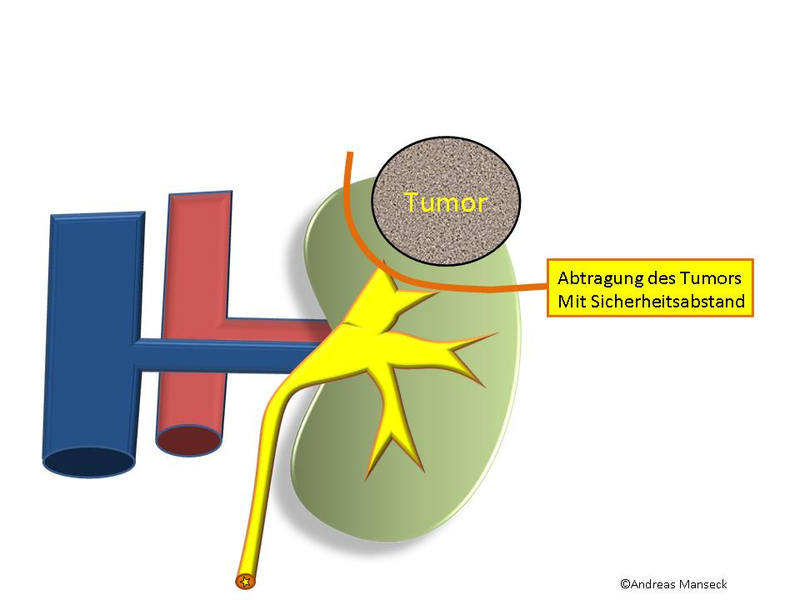
Nierenteilentfernung eines kleinen Nierentumors der linken Niere
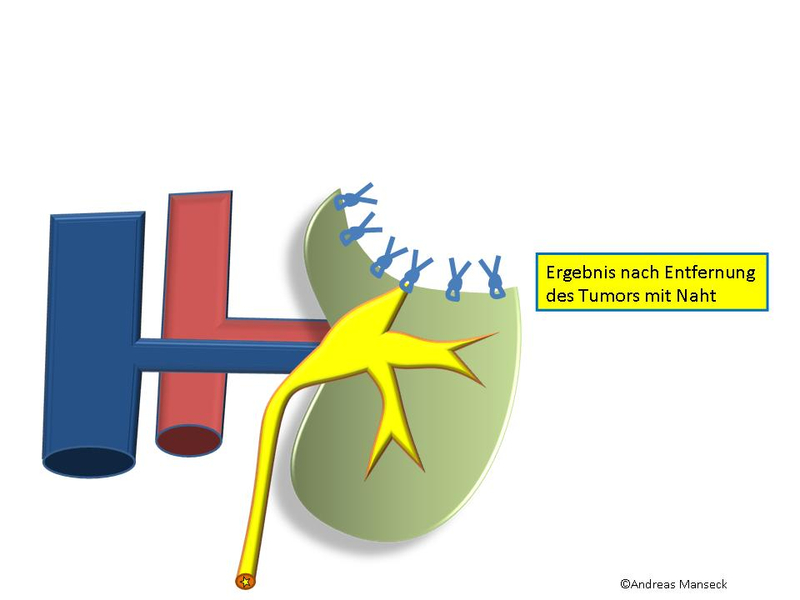
Ergebnis nach Entfernung des Tumors mit Naht
Metastasierte und fortgeschrittene Nierenzellkarzinome
Bei der Therapie metastasierter Nierenzellkarzinome steht die medikamentöse Behandlung im Vordergrund. Während bis 2006 nahezu ausschließlich die Immun- und Immunchemotherapie eingesetzt wurden, sind seither durch Zulassung verschiedenartiger neuer Substanzen individuellere Möglichkeiten gegeben. Es können also die jeweils vorliegenden Risiken in die Therapieplanung einbezogen werden.
Bei Nierentumoren, die die Niere verlassen haben und Absiedlungen in Lymphknoten oder anderen Organen (z.B. der Lunge) gesetzt haben, besteht in aller Regel keine Möglichkeit mehr, eine Heilung zu erzielen. Liegen bereits bei Diagnosestellung Tumorabsiedlungen außerhalb der Niere vor, kann jedoch die Entfernung der betroffenen Niere (palliative Tumornephrektomie) einen lebensverlängernden Effekt haben. Liegen nur einzelne Absiedlungen, z.B. in der Lunge oder im Knochen vor, sollte immer auch die Möglichkeit einer operativen Entfernung oder Bestrahlung überprüft werden. Lassen sich einzelne Metastasen chirurgisch entfernen oder durch eine Bestrahlung gut behandeln, ist dieser Weg einer medikamentösen Therapie vorzuziehen.
Bis zum Jahr 2006 standen als einzige effektive systemische Therapieformen die Immun- und die Immunchemotherapie zur Verfügung. Daneben waren auch zahlreiche unterstützende Möglichkeiten gegeben, so z.B. die Strahlentherapie bei schmerzhaften Knochenmetastasen oder bei der Gefahr des Knochenbruchs durch den Tumor.
Bei der Immun- bzw. Immunchemotherapie werden die Medikamente Interleukin-2 (IL-2) und/ oder Interferon-Alpha (IFN-alpha-2a) in Verbindung mit 5-Fluorouracil (einem Chemotherapeutikum) verabreicht.
Seit 2006 wurde die Immunchemotherapie zunehmend durch neue Substanzen verdrängt und wird derzeit kaum noch eingesetzt. Bei den neuen Substanzen sind vier verschiedene Gruppen verfügbar, die auf unterschiedlichen Ebenen das Tumorwachstum beeinflußen sollen. Aufgrund der Zulassung stehen derzeit für die Erstlinienbehandlung die Medikamente Avastin® in Kombination mit Interferon, Sutent® sowie Votrient® und für Patienten mit schlechterem Allgemeinbefinden Torisel® zur Verfügung. Patienten, die bereits wegen eines Nierenkrebses mit einem Medikament vorbehandelt wurden, können von der Behandlung mit Nexavar®, Inlyta®, Afinitor® oder Opdivo® profitieren.
Die Substanzgruppen:
- monoklonale Antikörper: Avastin®
- Tyrosinkinase-Inhibitoren: Sutent®, Nexavar®, Votrient®, Inlyta®
- mTOR-Inhibitoren: Torisel®, Afinitor®
- Checkpoint-Inhibitoren: Opdivo®
Sutent® (Sunitinib) beispielsweise hemmt mehrere Rezeptoren von Tyrosinkinasen, die für Wachstum und Blutgefäßbildung des Tumors wichtig sind. Das Medikament wird daher oft auch als Multikinaseinhibitor bezeichnet. Sorafenib (Nexavar®), Votrient®, Inlyta® haben einen ähnlichen Wirkmechanismus. Alle Medikamente führen häufig zu einer Stabilisierung der Erkrankung, teilweise auch mit einer Rückbildung der Absiedlungen verbunden. Im Unterschied zu den Immunchemotherapeutika werden mit den neuen Substanzen – die oft auch als TKI, small molecule drugs oder smart drugs bezeichnet werden – höhere Ansprechraten erzielt.
Seit 2007 steht eine weitere Substanz Temsirolimus (Torisel®) als Erstlinientherapie bei Nierenzellkarzinomen mit ungünstigen Prognoseeigenschaften zur Verfügung. Unter ungünstigen Prognoseeigenschaften versteht man dabei z. B. Patienten mit fortgeschrittener Erkrankung und deutlich eingeschränktem Allgemeinbefinden. Temsirolimus ist ein Medikament aus der Gruppe der mTOR-Hemmer, das zur Behandlung fortgeschrittener Nierenzellkarzinome eingesetzt wird. Temsirolimus hemmt das Protein mTOR, das in die Regulation des Zellwachstums und die Neubildung von Blutgefäßen eingebunden ist. Dadurch, dass Temsirolimus die Gefäßneubildung im Tumor unterdrückt, wird dessen Gewebe weniger durchblutet. Der Tumor kann nicht weiter wachsen. Temsirolimus verlängert das Überleben gegenüber der alleinigen Behandlung mit Interferon deutlich. Ein weiteres Medikament aus der Gruppe der mTOR-Inhibitoren wurde 2009 zugelassen. Everolimus (Afinitor®) ist nach Vorbehandlung mit einem Tyrosinkinaseinhibitor (TKI) zur Behandlung fortgeschrittener Nierenkrebserkrankungen angezeigt. Während Torisel® als Kurzinfusion verabreicht wird, kann Afinitor® als Tablette eingenommen werden.
Ebenfalls seit 2009 steht mit Bevacizumab (Avastin®) als sogenannter monoklonaler Antikörper in Verbindung mit der Gabe von Interferon-alpha- 2a eine weitere Möglichkeit in der Erstlinienbehandlung des metastasierten Nierenzellkarzinoms zur Verfügung.
Vorteil aller neuer Behandlungen für den Patienten ist die Krankheitsstabilisierung und das Verhindern des Auftretens von neuen Metastasen. Durch die Zulassung neuer Medikamente ist nun die Möglichkeit gegeben, den Tumor mit verschiedenen Substanzklassen, also auf verschiedenen Wegen zu bekämpfen. So steht beim Versagen des einen Medikaments immer noch ein anderes weiteres Medikament mit anderem Wirkprofil als effektive Behandlung zur Verfügung. Diese als Sequenztherapie bezeichnete, aufeinander folgende Behandlung mit verschiedenen Substanzen, kann bei ausgewählten Patienten die Überlebenszeit günstig beeinflussen.
Seit 2016 ist Nivolumab (Opdivo®) als neue Substanzklasse zur Therapie des Nierenzellkarzinoms zugelassen. Nivolumab stellt ein neues Immunonkologisches Konzept dar, das über die Stärkung der Körperabwehr wirkt. Auch hier ist die Zulassung derzeit bei Vorbehandlung des metastasierten Nierenzellkarzinoms gegeben.
Prognose
Das Nierenzellkarzinom ist eine schwere und lebensbedrohliche Krankheit. Die Heilungschancen sind von der Größe und der Ausbreitung des Tumors abhängig. Bei Patienten mit kleinen Tumoren ohne Metastasen beträgt die Fünf-Jahres-Überlebensrate bis zu 80 %.
Die Prognose ist stark vom Tumorstadium (also von der Tumorausdehnung) abhängig: